(SEBA)Secondary Education Board of AssamClass : XSubject : ScienceMedium : Assamese
Chapter : 3ধাতু আৰু অধাতু(Metals And Non-Metals)
অতিৰিক্ত প্ৰশ্নাৱলী :
ধৰ্মৰ ওপৰত ভিত্তি কৰি মৌলবোৰক কেইটা আৰু কি কি ভাগত ভাগ কৰা হৈছে?উত্তৰ : দুটা ভাগত ভাগ কৰা হৈছে।
(i) ধাতু
(ii) অধাতু
ধাতু আৰু অধাতুৰ পাৰ্থক্যবোৰ লিখা।
ধাতু আৰু অধাতুৰ ভৌতিক পাৰ্থক্যবোৰ লিখা।
ধাতু আৰু অধাতুৰ মাজৰ প্ৰভেদবোৰ লিখা।
উত্তৰ :
ধাতু—
ক) চিকমিকিয়া গুন/ দ্যুতি আছে।
খ) নমনীয়তা আৰু ঘাত সহনীয়তা গুন আছে।
গ) তাপ আৰু বিদ্যুতৰ সু-পৰিবাহী।
ঘ) টান বা কঠিন।
ঙ) নিনাদী গুন থাকে।
চ) গলনাংক উচ্চ।
ছ) কিছুমান ধাতুৰ নাম— Fe, Cu, Al, Mg, Zn আদি।
অধাতু—
ক) চিকমিকিয়া গুন/ দ্যুতি নাই।
খ) নমনীয়তা আৰু ঘাত সহনীয়তা গুন নাই।
গ) তাপ আৰু বিদ্যুতৰ কু-পৰিবাহী।
ঘ) গোটা বা কঠিন।
ঙ) গলনাংক কম।
চ) কিছুমান অধাতুৰ নাম— H, C, O, S, I, আদি
বৈদ্যুতিক তাঁৰৰ ওপৰত কিহৰ তৰপ দিয়া হয়?
উত্তৰ : PVC
PVC -ৰ সম্পূৰ্ণ নাম লিখা।
উত্তৰ : Polyvinyl chloride (পলিভিলাইন ক্ল'ৰাইড)
Note :
• পাৰাৰ বাহিৰে সকলোবোৰ ধাতু সাধাৰণ উষ্ণতাত গোটা কঠিন।
• গেলিয়াম আৰু ছিজিয়ামৰ বাহিৰে সকলোবোৰ ধাতুৰ গলনাংক উচ্চ।
• আয়ডিন অধাতু কিন্তু দ্যুতি আছে।
• হীৰা অধাতু কিন্তু গলনাংক উচ্চ।
• গ্ৰেফাইট অধাতু কিন্তু বিদ্যুতৰ সু-পৰিবাহী।
• লিথিয়াম, ছডিয়াম, পটাছিয়াম আদি ক্ষাৰ ধাতু গলনাংক কম, কোমল, কটাৰীৰে কাটিব পাৰি।
কাৰ্বনৰ বহুৰূপ কি? দুটা বহু ৰূপৰ নাম লিখা।
উত্তৰ : কাৰ্বন এটা অধাতু, ই বেলেগ বেলেগ অৱস্থাত থাকিব পাৰে। কাৰ্বনৰ এই প্ৰতিটো অৱস্থাক বহুৰূপ বোলে।
কাৰ্বনৰ বহু ৰূপৰ নাম -
ক) হীৰা
খ) গ্ৰেফাইট
অধিক জানিবলৈ :
( "অধ্যায়— ৫" আধুনিক পৰ্যাবৃত্ত তালিকা চোৱা)মাৰকিউৰি ধাতুৰ চিহ্ন আৰু আন এটা নাম লিখা।
উত্তৰ :
চিহ্ন →Hg
নাম → পাৰা
ৰূপৰ চিহ্ন আৰু নাম লিখা।
উত্তৰ :
চিহ্ন → Ag
নাম → ছিলভাৰ
সোণৰ চিহ্ন আৰু নাম লিখা।
উত্তৰ :
চিহ্ন → Au
নাম → গোল্ড
তামৰ চিহ্ন আৰু নাম লিখা।
উত্তৰ :
চিহ্ন → Cu
নাম → কপাৰ
সীহৰ চিহ্ন আৰু নাম লিখা।
উত্তৰ :
চিহ্ন → Pb
নাম → লেড
লোৰ চিহ্ন আৰু নাম লিখা।
উত্তৰ :
চিহ্ন → Fe
নাম → আইৰন
পাঠভিত্তিক প্ৰশ্নাৱলী : পৃষ্ঠা - 40
1.ধাতু একোটাৰ উদাহৰণ দিয়া যি ধাতু -(i) সাধাৰণ উষ্ণতাত জুলীয়া। [HSLC.'17]
(ii) কটাৰিৰে সহজে কাটিব পাৰি।
(iii) তাপৰ আটাইতকৈ সুপৰিবাহী।
(iv) তাপৰ কম পৰিবাহী। [HSLC.'22]
উত্তৰ :
(i) পাৰা (Hg)
(ii) Li / Na / K
(iii) ৰূপ / তাম
(iv) সীহ / পাৰা
2. ধাতুৰ ঘাত সহনীয়তা আৰু নমনীয়তাৰ অর্থ বহলাই আলোচনা কৰা।
উত্তৰ :
ধাতুৰ ঘাত সহনীয়তা :
কিছুমান ধাতু হাতুৰিৰে মৰিয়াই পাতল পাত এচটা বনাব পাৰি। এই ধৰ্মক ধাতুৰ ঘাত সহনীয়তা বোলে।
যেনে - সোণ, ৰূপ।
ধাতুৰ নমনীয়তা :
ধাতুৰ পাত দীঘল কৰি তাঁৰলৈ পৰিৱৰ্তন কৰিব পৰা গুণকে নমনীয়তা বোলে।
যেনে - সোণ।
• এক গ্রাম সোণৰ পৰা 2km দৈর্ঘ্যৰ তাঁৰ পাব পাৰি।
ধাতুৱে অক্সিজেনৰ লগত বিক্ৰিয়া কৰিলে কি উৎপন্ন হয়? উদাহৰণ দিয়া।
উত্তৰ : ধাতুৱে অক্সিজেনৰ লগত বিক্ৰিয়া কৰি ধাতৱ অক্সাইড উৎপন্ন কৰে।
উদাহৰণ—
i) 2Cu+O₂→2CuO
ii) 4Al+3O₂→2Al₂O₃
উভধৰ্মী অক্সাইড কাক বোলে? উদাহৰণ দিয়া।
উত্তৰ : যিবোৰ ধাতৱ অক্সাইড অম্ল আৰু ক্ষাৰ উভয়ৰে লগত বিক্রিয়া কৰি লৱন আৰু পানী উৎপন্ন কৰে তাক উভধৰ্মী অক্সাইড বোলে।
উদাহৰণ : Al₂O₃+6HCL→2AlCl+3H₂O
ছ’ডিয়াম আৰু পটাছিয়ামৰ দৰে ধাতুবোৰক কেৰাচিন তেলত ডুবাই ৰখা হয় কিয়?
উত্তৰ : কাৰণ— মুক্ত বায়ুত বিক্ৰিয়া ঘটিল জুই জ্বলি উঠে। দুৰ্ঘটনা ৰোধ কৰিবলৈ সিহঁতক কেৰাচিন তেলত ডুবাই ৰখা হয়।
Note :
ৰূপ (Silver) আৰু সোণ (gold) উচ্চ উষ্ণতাতো অক্সিজেনৰ লগত বিক্রিয়া নকৰে।
ধাতুৱে পানীৰ লগত বিক্ৰিয়া কৰিলে কি উৎপন্ন হয়? উদাহৰণ দিয়া।
উত্তৰ : ধাতুৱে পানীৰ লগত বিক্ৰিয়া কৰি ধাতৱ অক্সাইড আৰু হাইড্ৰ'জেন গেছ উৎপন্ন কৰে।
উদাহৰণ—
i) 2K+2H₂O→2KOH
ii) 2Na+2H₂O→2NaOH
ধাতুৱে এছিডৰ লগত বিক্ৰিয়া কৰিলে কি উৎপন্ন হয়? উদাহৰণ দিয়া।
উত্তৰ : ধাতুৱে এছিডৰ লগত বিক্ৰিয়া কৰি লৱন আৰু পানী উৎপন্ন কৰে।
উদাহৰণ—
i) Zn+HCl→ZnCl₂+H₂
ii) Al+HCl→2AlCl₃+3H₂
iii) Mg+HCl→MgCl₂+H₂
iv) Fe+HCl→FeCl₂+H₂
ধাতুৰ সক্ৰিয়তাৰ ক্ৰম :
পাঠভিত্তিক প্ৰশ্নাৱলী : পৃষ্ঠা - 46
1. ছডিয়াম ধাতু কিয় কেৰাচিন তেলত ডুবাই ৰখা হয়? [HSLC.'15]উত্তৰ : ছডিয়াম আটাইতকৈ সক্ৰিয় ধাতু। এনে ধাতুৱে ইমান প্ৰৱণতাৰে বিক্ৰিয়া কৰে যে মুক্ত বায়ুত বিক্রিয়া ঘটিলে জুই জ্বলি উঠে আৰু এনে দুৰ্ঘটনা ৰোধ কৰিবলৈ ছডিয়াম ধাতু কেৰাচিন তেলত ডুবাই ৰখা হয়।
উত্তৰ : 3Fe+4H₂O → Fe₃O₄+4H₂
(ii) পানীৰ লগত কেলছিয়াম আৰু পটাছিয়ামৰ বিক্রিয়া। [HSLC.'15,'22]
উত্তৰ :
•পানীৰ লগত কেলছিয়ামৰ বিক্রিয়া :
Ca+2H₂O → Ca(OH)₂+H₂
•পানীৰ লগত পটাছিয়ামৰ বিক্রিয়া :
2K+H₂O → 2KOH+H₂+তাপ শক্তি
3. A, B, C, D চাৰিটা ধাতু লৈ তলৰ দ্ৰৱণ বিলাকত এটা এটাকৈ দিয়া হৈছিল। ফলাফলবিলাক তলৰ তালিকাত লিপিবদ্ধ কৰা হৈছে।
(i) আটাইতকৈ সক্রিয় ধাতু কোনটো?
(ii) কপাৰ (II) ছালফেট লৱণত B ধাতু দিলে কি হ'ব?
(ii) A B C D ধাতুক সক্ৰিয়তাৰ নিম্নক্রমত সজোৱা।
উত্তৰ :
(i) B
(ii) প্ৰতিষ্ঠাপন বিক্ৰিয়া ঘটিব।
(iii) B>A>C>D
Note :
অধিক জানি লওঁ আহা :
∵ তালিকাটোত দিয়া ফলাফলবিলাকত ধাতুৰ সক্ৰিয়তাৰ ক্ৰম হ' ল = জিংক>আইৰণ>কপাৰ>ছিলভাৰ।
আৰু A B C D ধাতুৰ ভিতৰত B ধাতুৱে আইৰণক প্ৰতিষ্ঠাপন (আতৰ) কৰিলে। সেয়ে, আটাইতকৈ সক্রিয় ধাতু হ' ব = B
∵ B আটাইতকৈ সক্রিয় ধাতু।
∴ কপাৰ (II) ছালফেট লৱণত B ধাতু দিলে কপাৰক প্ৰতিষ্ঠাপিত (আতৰ) কৰিব।
ধাতুৰ সক্ৰিয়তাৰ ক্ৰমৰ পৰা,
∵ ধাতু, B য়ে আইৰণ, A য়ে কপাৰ, C য়ে ছিলভাৰক প্ৰতিষ্ঠাপন কৰিলে আৰু D কোনো বিক্রিয়া নহ' ল।
∴ B>A>C>D
নিম্নক্রমত সজোৱা = ডাঙৰৰ পৰা সৰুলৈকে সজোৱা।
4. লঘু হাইড্ৰ’ক্লৰিক এছিড (HCl) ত এটা সক্ৰিয় ধাতু দিলে কি গেছ উৎপন্ন হয় ? আইৰণে লঘু (H₂SO₄) ৰ লগত কৰা বিক্ৰিয়াটোৰ সমীকৰণ লিখা। [HSLC.'22]
উত্তৰ : H₂ গেছ উৎপন্ন হয়।
বিক্ৰিয়াটোৰ সমীকৰণ :
Fe+H₂SO₄ → FeSO₄+H₂
5. আইৰণ (II) ছালফেট দ্ৰৱণত যিংক ধাতু দিলে কি দেখিবা ? সংঘটিত হোৱা বিক্ৰিয়াটো লিখা । [HSLC.'18, '22]
উত্তৰ :
যিংকে আইৰণ ছালফেটৰ পৰা আইৰণক অপসাৰিত কৰি যিংক ছালফেট আৰু আইৰণ উৎপন্ন কৰিব। ফলত আইৰণ ছালফেটৰ সেউজীয়া বৰণ ক্ৰমে নাইকিয়া হ’ব।
সংঘটিত হোৱা বিক্ৰিয়াটো :-
Zn+FeSO₄ → ZnSO₄+Fe
অতিৰিক্ত প্ৰশ্নাৱলী :
ইলেকট্ৰনৰ স্থানান্তৰৰ জৰিয়তে ছডিয়াম ক্লৰাইড (NaCl) -ৰ গঠন লিখা।উত্তৰ :
Note :
অধিক জানি লওঁ আহা :
Na₁₁ : 2,8,1
ইয়াত, ছ’ডিয়ামৰ বহিৰতম কক্ষত 1 টা ইলেক্ট্রন আছে। এটা ধনাত্মক আধান বেছি আছে। ই এটা ইলেক্ট্রন এৰি দি সুস্থিৰ অষ্টক বিন্যাস লাভ কৰিব। সেয়ে আমি এটা ছ’ডিয়াম কেটায়ন (Na⁺) পাওঁ।
Cl₁₇ : 2,8,7
ইয়াত, ক্ল'ৰিনৰ বহিৰতম কক্ষত 7 টা ইলেক্ট্রন আছে। ই এটা ইলেক্ট্রন গ্রহণ কৰি সুস্থিৰ অষ্টক বিন্যাস লাভ কৰিব।
ছ’ডিয়াম আৰু ক্ল'ৰিনৰ বিক্ৰিয়া ঘটিলে ছ’ডিয়ামে এৰি দিয়া ইলেক্ট্ৰনটো ক্ল'ৰিনে গ্ৰহণ কৰে। ইলেক্ট্ৰনটো গ্ৰহণ কৰি ক্ল'ৰিনৰ পৰমাণুটো ঋণাত্মক আধানযুক্ত হৈ পৰে, এইদৰে ক্ল'ৰাইড এনায়ন (Cl⁻) সৃষ্টি হয়।
ইলেকট্ৰনৰ স্থানান্তৰৰ জৰিয়তে মেগনেছিয়াম ক্লৰাইড (MgCl₂) -ৰ গঠন লিখা।
উত্তৰ :
Note :
অধিক জানি লওঁ আহা :
Mg₁₂ : 2,8,2
ইয়াত, মেগনেছিয়ামৰ বহিৰতম কক্ষত 2 টা ইলেক্ট্রন আছে। দুটা ধনাত্মক আধান বেছি আছে। ই এটা ইলেক্ট্রন এৰি দি সুস্থিৰ অষ্টক বিন্যাস লাভ কৰিব। সেয়ে আমি এটা ছ’ডিয়াম কেটায়ন (Mg²⁺) পাওঁ।
Cl₁₇ : 2,8,7
ইয়াত, ক্ল'ৰিনৰ বহিৰতম কক্ষত 7 টা ইলেক্ট্রন আছে। ই এটা ইলেক্ট্রন গ্রহণ কৰি সুস্থিৰ অষ্টক বিন্যাস লাভ কৰিব।
Mg আৰু Cl₂ -ৰ বিক্ৰিয়া ঘটিলে Mg এৰি দিয়া ইলেক্ট্ৰনবোৰ দুটা ক্ল'ৰিনে গ্ৰহণ কৰে। ইলেক্ট্ৰনবোৰ গ্ৰহণ কৰি ক্ল'ৰিনৰ পৰমাণুটো ঋণাত্মক আধানযুক্ত হৈ পৰে, এইদৰে ক্ল'ৰাইড এনায়ন (Cl⁻) সৃষ্টি হয়।
আয়নীয় যৌগ কাক বোলে?
ইলেক্ট্ৰ'যোগী যৌগ কাক বোলে?
উত্তৰ : যিবোৰ যৌগ হলেক্ট্ৰনৰ স্থানান্তৰণৰ ফলত
গঠন হয়, সেইবোৰক আয়নীয় বা ইলেক্ট্ৰ'যোগী যৌগ বোলে।
MgCl₂ -ত কেটায়ন আৰু এনায়ন দুটাৰ নাম লিখা।
উত্তৰ :
কেটায়ন : Mg²⁺
এনায়ন : Cl⁻
আয়নীয় যৌগৰ ধর্মবোৰ লিখা।
উত্তৰ :
(i) কঠিন বা গোটা আৰু কিছু দৃঢ়।
(ii) গলনাংক আৰু উতলাংক উচ্চ।
(iii) পানীত দ্রৱণীয় কিন্তু কেৰাচিন, পেট্ৰ'ল আদিত অদ্রৱণীয়।
(iv) কঠিন অৱস্থাত বিদ্যুৎ পৰিবহন নকৰে।
(v) বিগলিত বা জলীয় অৱস্থাত বিদ্যুৎ পৰিবহন কৰে।
আয়নীয় যৌগবোৰে কঠিন অৱস্থাত বিদ্যুৎ পৰিবহন নকৰে, কিন্তু বিগলিত বা জলীয় অৱস্থাত বিদ্যুৎ পৰিবহন কৰে কিয়?
উত্তৰ :
কঠিন অৱস্থাত বিদ্যুৎ পৰিবহন নকৰে; কাৰণ- ইহঁতৰ দৃঢ় গঠনৰ বাবে আয়নবোৰ লৰচৰ কৰিব নোৱাৰে।
বিগলিত বা জলীয় অৱস্থাত বিদ্যুৎ পৰিবহন কৰে; কাৰণ- বিগলিত অৱস্থাত বিপৰীত ধর্মী আয়নবোৰৰ মাজৰ আকর্ষণী শক্তিৰ তুলনাত প্রয়োগ কৰা তাপশক্তিৰ মান অধিক হয় । ফলত আয়নবোৰ চলাচল কৰিবলৈ মুক্ত হয় আৰু এই আয়নবোৰেই বিদ্যুৎ পৰিবহন কৰে।
পাঠভিত্তিক প্ৰশ্নাৱলী : পৃষ্ঠা - 49
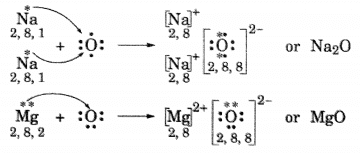
1. (i) ছডিয়াম, অক্সিজেন আৰু মেগনেছিয়ামৰ ইলেকট্ৰন বিন্দু গঠন লিখা।(ii) ইলেকট্ৰনৰ স্থানান্তৰৰ জৰিয়তে Na₂O আৰু MgO ৰ গঠন লিখা।
(iii) এই যৌগটোত থকা আয়নসমূহ কি কি?
উত্তৰ :
(i)
(ii)
উত্তৰ : কাৰণ— আয়নীয় যৌগবোৰৰ আন্তঃআয়নীয় বিদ্যুত স্থিতীয় আকৰ্ষণ বল অতি বেছি। ফলত আয়নসমূহ পৃথক কৰিবলৈ যথেষ্ট তাপ শক্তি প্ৰয়োজন।
অতিৰিক্ত প্ৰশ্নাৱলী :
মণিক কিখনিজ পদার্থ কাক বোলে?
উত্তৰ :
পৃথিৱীত মৌল বা যৌগ অৱস্থাত ভূত্বকত পোৱা পদার্থবোৰক খনিজ পদার্থ বা মণিক বুলি কোৱা হয়।
আকৰ কাক বোলে?
উত্তৰ :
কিছুমান খনিজ পদার্থত কোনো এবিধ ধাতুৰ পৰিমাণ অধিক থাকে আৰু তাৰ পৰা ধাতুবিধ লাভজনকভাৱে আহৰণ কৰিব পাৰি। এই ধৰণৰ খনিজ পদার্থবিধক ধাতুটোৰ আকৰিক বা আকৰ বুলি কোৱা হয়।
প্ৰাকৃতিত মুক্ত অৱস্থাত পোৱা ধাতুবোৰ কি কি?
উত্তৰ : গোল্ড, ছিলভাৰ, প্লেটিনাম, কপাৰ আদি।
খনিজ মল কাক বোলে?
উত্তৰ : খনিৰ পৰা আহৰণ কৰা সময়ত আকৰৰ লগত বহুতো অশুদ্ধি (যেনে মাটি, বালি আদি) মিহলি হৈ থাকে । এই অশুদ্ধি বা অপদ্ৰৱ্যবোৰক খনিজ মল বোলে।
তাপজাৰণ কাক বোলে? ৰাসায়নিক সমীকৰণ এটাৰ দ্বাৰা ব্যাখ্যা কৰা । [HSLC.'16]
উত্তৰ : অতিৰিক্ত বায়ুৰ উপস্থিতিত উচ্চ তাপত উত্তপ্ত কৰি ছালফাইড আকৰক ধাতৱ অক্সাইডলৈ ৰূপান্তৰিত কৰা হয়। এই প্ৰক্ৰিয়াক তাপজাৰণ বোলে ।
যেনে—
2ZnS + 30₂ → 2ZnO + 2SO₂
দগ্ধীকৰণ কাক বোলে ? এটা উদাহৰণৰ সৈতে বুজাই লিখা ।
উত্তৰ : পৰিমিত বায়ুৰ পৰিৱেশত উচ্চ তাপত উত্তপ্ত কৰি কাৰ্বনেট আকৰক ধাতৱ অক্সাইডলৈ ৰূপান্তৰিত কৰা হয়। এই প্ৰক্ৰিয়াক দগ্ধীকৰণ বোলে ৷
যেনে—
ZnCO₃ তাপ → ZnO + CO₂
তলত দিয়া বিক্ৰিয়াটোত জাৰিত আৰু বিজাৰিত হোৱা পদাৰ্থটো উলিওৱা।
3 MnO₂(s) + 4Al(s) → 3Mn(l) + 2Al₂O₃(s) + তাপ
উত্তৰ : ইয়াত,
Al জাৰিত হৈছে।
MnO₂ বিজাৰিত হৈছে।
অক্সাইডৰ পৰা ধাতু উৎপন্ন কৰিবলৈ কি ৰাসায়নিক পদ্ধতি প্ৰয়োগ কৰা হয়? উদাহৰণেৰে সৈতে ব্যাখ্যা কৰা হয়। [HSLC.'20]
উত্তৰ : বিজাৰণ পদ্ধতি পদ্ধতি প্ৰয়োগ কৰা হয়।
উদাহৰণ : যিংক অক্সাইড কার্বনৰ লগত উত্তপ্ত কৰিলে ধাতৱ যিংকলৈ বিজাৰিত হয়।
ZnO + C তাপ → Zn + CO
থার্মিট বিক্রিয়া কি ? থার্মিট বিক্ৰিয়াৰ সন্তুলিত সমীকৰণ লিখা। [ HSLC.'23]
উত্তৰ :
থার্মিট বিক্রিয়া : আইৰণ (III) অক্সাইড (Fe₂O₃) ৰ লগত এলুমিনিয়ামৰ বিক্ৰিয়াটো অতিশয় তাপবৰ্জী বিক্ৰিয়া আৰু বিক্ৰিয়াত উৎপন্ন হোৱা আইৰণ বিগলিত অৱস্থাত পোৱা যায়। ইয়াক থাৰ্মিট বিক্ৰিয়া বোলে।
থার্মিট বিক্ৰিয়াৰ সন্তুলিত সমীকৰণ :
Fe₂O₃ + 2Al → 2Fe + Al₂O₃ + তাপ
থার্মিট বিক্রিয়াৰ দুটা ব্যৱহাৰ লিখা।
উত্তৰ :
ক) ৰেল লাইন জোৰা দিবলৈ।
খ) যন্ত্র-পাতিৰ ভগা অংশ জোৰা লগাবলৈ।
পাঠভিত্তিক প্ৰশ্নাৱলী : পৃষ্ঠা - 53
1. তলত দিয়াবোৰৰ সংজ্ঞা লিখা। [HSLC.'20](i) মণিক (mineral) (ii) আকৰ (ore) (iii) খনিজ মল (gangue)
উত্তৰ :
(i) মণিক : পৃথিৱীত মৌল বা যৌগ অৱস্থাত ভূত্বকত পোৱা পদার্থবোৰক খনিজ পদার্থ বা মণিক বুলি কোৱা হয়।
(ii) আকৰ : কিছুমান খনিজ পদার্থত কোনো এবিধ ধাতুৰ পৰিমাণ অধিক থাকে আৰু তাৰ পৰা ধাতুবিধ লাভজনকভাৱে আহৰণ কৰিব পাৰি। এই ধৰণৰ খনিজ পদার্থবিধক ধাতুটোৰ আকৰিক বা আকৰ বুলি কোৱা হয়।
(iii) খনিজ মল : খনিৰ পৰা আহৰণ কৰা সময়ত আকৰৰ লগত বহুতো অশুদ্ধি (যেনে মাটি, বালি আদি) মিহলি হৈ থাকে । এই অশুদ্ধি বা অপদ্ৰৱ্যবোৰক খনিজ মল বোলে।
2. প্ৰকৃতিত মুক্ত অৱস্থাত পোৱা দুটা ধাতুৰ নাম লিখা। [HSLC.'17]
উত্তৰ : গোল্ড, ছিলভাৰ।
3. অক্সাইডৰ পৰা ধাতু উৎপন্ন কৰিবলৈ কি ৰাসায়নিক পদ্ধতি প্ৰয়োগ কৰা হয় ? [HSLC.'20]
উত্তৰ : বিজাৰণ পদ্ধতি।
অতিৰিক্ত প্ৰশ্নাৱলী :
লোত মামৰ ধৰা ৰোধ কৰা পদ্ধতিবোৰ লিখা।উত্তৰ :
i) ৰঙ কৰা (painting),
ii) তেল সনা (oiling),
iii) গ্রীজসনা (greesing),
iv) দস্তালেপন (galvanising),
v) ক্র’মপ্লেটিং (chrome plating),
দস্তালেপন পদ্ধতি কি?
উত্তৰ : দস্তালেপন হ'ল ষ্টিল আৰু লোত মামৰ নধৰিবৰ বাবে যিংকৰ আৱৰণ দিয়া এটা পদ্ধতি ।
সংকৰ ধাতু (alloy) কি?
সংকৰ ধাতু কাক বোলে?
উত্তৰ : সংকৰ ধাতু হ'ল দুটা বা ততোধিক ধাতু নাইবা এটা ধাতু আৰু এটা অধাতুৰ সমসত্ব মিশ্রণ।
এমালগাম কাক বোলে?
উত্তৰ : সংকৰ ধাতুৰ এটা উপাদানত পাৰা হ'লে তাক এমালগাম বোলা হয়।
পাঠভিত্তিক প্ৰশ্নাৱলী : পৃষ্ঠা - 55
1. যিংক, মেগনেছিয়াম আৰু কপাৰৰ ধাতৱ অক্সাইড তলত দিয়া ধাতুবোৰৰ লগত উত্তপ্ত কৰা হ'ল।কোনবিলাক ক্ষেত্ৰত প্ৰতিষ্ঠাপন বিক্রিয়া ঘটিব?
উত্তৰ :
প্ৰতিষ্ঠাপন বিক্রিয়া ঘটিব :
যিংক অক্সাইডৰ লগত মেগনেছিয়াম দিলে।
কপাৰ অক্সাইডৰ লগত জিংক, মেগনেছিয়াম দিলে।
2. কোনবোৰ ধাতু সহজে ক্ষয় নহয় ?
উত্তৰ : সোণ আৰু প্লেটিনাম।
3. সংকৰ ধাতু কি?
উত্তৰ : দুটা বা ততোধিক ধাতু নাইবা এটা ধাতু আৰু এটা অধাতুৰ সমসত্ব মিশ্রণক সংকৰ ধাতু বোলে।
পাঠভিত্তিক প্ৰশ্নাৱলী : পৃষ্ঠা - 56
1. তলৰ কোনবোৰৰ ক্ষেত্ৰত প্ৰতিস্থাপন বিক্ৰিয়া ঘটিব ?(a) NaCl ৰ দ্ৰৱ আৰু কপাৰ ধাতু।
(b) MgCl₂ ৰ দ্ৰৱ আৰু এলুমিনিয়াম ধাতু।
(c) FeSO₄ ৰ দ্ৰৱ আৰু ছিলভাৰ ধাতু।
(d) AgNO₃ ৰ দ্ৰৱ আৰু কপাৰ ধাতু।
উত্তৰ : (d) AgNO₃ ৰ দ্ৰৱ আৰু কপাৰ ধাতু।
2. লোৰ টাৱা (iron frying pan) এখন মামৰে ধৰাৰ পৰা বচাই ৰাখিবলৈ তলৰ কোনটো পদ্ধতি উপযুক্ত হ’ব? [HSLC.'20]
(a) গ্ৰীজ ব্যৱহাৰ কৰি।
(b) ৰং ব্যৱহাৰ কৰি।
(c) যিংকৰ প্ৰলেপ দি।
(d) ওপৰৰ সকলো।
উত্তৰ : (c) যিংকৰ প্ৰলেপ দি।
3. এটা মৌলই অক্সিজেনৰ লগত বিক্ৰিয়া কৰি উচ্চ গলনাংকৰ যৌগ উৎপন্ন কৰে। যৌগটো পানীত দ্ৰৱণীয়। সম্ভৱপৰ মৌলটো লিখা। [HSLC.'19,'22]
(a) কেলছিয়াম
(b) কাৰ্বন
(c) ছিলিকন
(d) আইৰন
উত্তৰ : (a) কেলছিয়াম।
4. খাদ্যবস্তু ভৰাই ৰখা পাত্ৰবোৰত টিনৰ প্ৰলেপ দিয়া হয়, যিংকৰ নহয়। কিয়নো— [HSLC.'18]
(a) টিনতকৈ যিংক দামী।
(b) যিংকৰ গলনাংক টিনতকৈ বেছি।
(c) যিংক টিনতকৈ অধিক সক্ৰিয়।
(d) যিংক টিনতকৈ কম সক্ৰিয়।
উত্তৰ : (c) যিংক টিনতকৈ অধিক সক্ৰিয়।
5. তোমাক এটা হাতুৰী, এটা বেটাৰী, অলপ তাৰ আৰু এটা ছুইচ দিয়া হ’ল।
(a) এই বস্তুবোৰ ব্যৱহাৰ কৰি ধাতু আৰু অধাতু কেনেকৈ চিনাক্ত কৰিবা ?
(b) ধাতু/অধাতুৰ চিনাক্তকৰণত এই পৰীক্ষাবোৰৰ উপযোগিতা উল্লেখ কৰিবা। [HSLC.'15,'19]
উত্তৰ :
(a) হাতুৰীৰে পিটিলে ধাতু পাতল হ’ব। আনহাতে অধাতু গুড়ি হ'ব। আকৌ বেটাৰী, বাল্ব, তাঁৰ আৰু ছুইচ সংযোগ কৰা হয়, তেতিয়া ধাতুৰ মাজেৰে প্ৰবাহ পাৰ হৈ যায়। আনহাতে অধাতুৰ মাজেৰে প্ৰবাহ পাৰ হৈ নাযায়।
(b) নমনীয়তাৰ বাবে ধাতুবোৰক আমাৰ সুবিধা অনুযায়ী পাতল পাতৰ আকৃতি বনাব পাৰি। ধাতুবোৰ বিদ্যুতৰ সুপৰিবাহী বাবে বৈদ্যুতিক তাঁৰ বনাবলৈ ব্যৱহাৰ কৰিব পাৰি।
6. উভধৰ্মী অক্সাইড কাক বোলে? দুটা উভধৰ্মী অক্সাইডৰ নাম লিখা। [HSLC.'19,'22]
উত্তৰ : যিবোৰ ধাতৱ অক্সাইড অম্ল আৰু ক্ষাৰ উভয়ৰে লগত বিক্রিয়া কৰি লৱন আৰু পানী উৎপন্ন কৰে তাক উভধৰ্মী অক্সাইড বোলে।
উদাহৰণ :
i) এলুমিনিয়াম অক্সাইড।
ii) যিংক অক্সাইড।
i) Al₂O₃+6HCL→2AlCl+3H₂O
ii) ZnO+2HCl → ZnCl₂+H₂O
7. দুটাকৈ ধাতুৰ নাম লিখা যিয়ে লঘু এছিডৰপৰা হাইড্ৰজেন অপসৰণ কৰে আৰু যিয়ে নকৰে।
উত্তৰ :
অপসৰণ কৰে : Mg, Fe
অপসৰণ নকৰে : Cu, Si
8. M ধাতুৰ বৈদ্যুতিক শোধনৰ বেলিকা এনড, কেথড আৰু বিদ্যুত বিশ্লেষ্য কি ল’ব লাগিব ?
উত্তৰ :
অশুদ্ধ ধাতু M → এন’ডত জমা হ’ব।
বিশুদ্ধ ধাতু M → কেথ’ডত জমা হ’ব।
বিদ্যুত বিশ্লেষ্য M → ধাতুৰ লৱনৰ এটা দ্ৰৱ।
9. প্ৰত্যুষে সৰু চামুচ এখনত ছালফাৰ গুড়ি লৈ উত্তাপিত কৰিলে l উদ্ভৱ হোৱা গেছটো এটা পৰীক্ষানলী ওভোতাকৈ ধৰি সংগ্ৰহ কৰিলে।
(a)
(i) শুষ্ক লিটমাছ কাগজৰ লগত
(ii) সিক্ত লিটমাছ কাগজৰ লগত গেছটোৰ বিক্ৰিয়া কেনে হ’ব?
(b) ইয়াত বিক্ৰিয়াটোৰ সন্তুলিত সমীকৰণ লিখা। [HSLC.'17,'19]
উত্তৰ :
(a)
(i) কোনো বিক্ৰিয়া নকৰে।
(ii) ৰঙা ৰঙলৈ পৰিৱৰ্তন কৰিব।
(b) সন্তুলিত সমীকৰণটো :
SO₂+H₂O → H₂SO₃
10. লোত মামৰে ধৰা ৰোধ কৰিবলৈ দুটা উপায় বৰ্ণনা কৰা। [HSLC.'19]
উত্তৰ :
(i) ৰং কৰা।
(ii) দস্তালেপন।
11. অক্সিজেনৰ লগত বিক্ৰিয়া কৰি অধাতুবিলাকে কেনে অক্সাইড উৎপন্ন কৰে? [HSLC.'17]
উত্তৰ : আম্লিক অক্সাইড।
12. কাৰণ দৰ্শোৱা :
(a) গহনা তৈয়াৰ কৰিবলৈ প্লেটিনাম, গল্ড আৰু ছিলভাৰ ব্যৱহাৰ কৰা হয়।
উত্তৰ : কাৰণ— এইবোৰ অতিকৈ নিষ্ক্ৰিয় ধাতু, সহজে ক্ষয় নহয়।
(b) ছডিয়াম, পটাছিয়াম আৰু লিথিয়াম ধাতু তেলত ডুবাই ৰখা হয়।
উত্তৰ : কাৰণ— এইবোৰ আটাইতকৈ সক্ৰিয় ধাতু। এনে ধাতুৱে মুক্ত বায়ুত বিক্রিয়া ঘটি জুই জ্বলি উঠে আৰু এনে দুৰ্ঘটনা ৰোধ কৰিবলৈ কেৰাচিন তেলত ডুবাই ৰখা হয়।
(c) এলুমিনিয়াম যথেষ্ট সক্ৰিয় ধাতু তথাপি ইয়াক ৰন্ধনত ব্যৱহাৰ কৰা বৰ্তন তৈয়াৰ কৰিবলৈ ব্যৱহাৰ কৰা হয়।
উত্তৰ : কাৰণ— এলুমিনিয়াম তাপৰ সুপৰিবাহী। ই বায়ুত থকা অক্সিজেনৰ লগত বিক্ৰিয়া কৰি এলুমিনিয়াম অক্সাইডৰ আৱৰণ পৰে। ই ক্ষয়ীভৱনৰ পৰা ৰক্ষা কৰে।
(d) ধাতু নিষ্কাষণৰ সময়ত কাৰ্বনেট আৰু ছালফাইড আকৰ অক্সাইডলৈ ৰূপান্তৰ কৰা হয়। [HSLC.'15,'18]
উত্তৰ : কাৰণ— ধাতুৰ অক্সাইডৰ পৰা ধাতু নিষ্কাষণ কৰা অতি সহজ।
13. চেকালগা কপাৰৰ পাত্ৰ নেমু বা তেতেলী ৰসেৰে পৰিষ্কাৰ কৰা দেখিছানে? পাত্ৰবিলাক পৰিষ্কাৰ কৰিবলৈ টেঙাজাতীয় বস্তু কিয় বাৱহাৰ কৰে? [HSLC.'20]
উত্তৰ : কাৰণ— টেঙাজাতীয় পদার্থত এচিড থাকে। কপাৰ, কাৰ্বনেটৰ এটা প্ৰলেপ। এই কপাৰ কাৰ্বনেট এচিডত দ্ৰৱীভূত হয়। ফলত কপাৰৰ পাত্ৰৰ পৃষ্ঠৰ পৰা চেকাবোৰ আঁতৰি যায়।
14. ৰাসায়নিক ধৰ্মৰ ভিত্তিত ধাতু আৰু অধাতুৰ পাৰ্থক্য লিখা।
উত্তৰ :
ধাতু :
(i) ক্ষাৰকীয় অক্সাইড গঠন।
(ii) আয়নীয় প্ৰকৃতি।
(iii) ধণাত্মক আধান উৎপন্ন কৰে।
(iv) হাইড্ৰ’জেন অপসাৰিত কৰে।
অধাতু :
(i) আম্লিক অক্সাইড গঠন কৰে।
(ii) সহযোজী প্ৰকৃতি।
(iii) ঋণাত্মক আধান উৎপন্ন কৰে।
(iv) হাইড্ৰ’জেন অপসাৰিত কৰিব নোৱাৰে।
15. এজন ভণ্ড মানুহ স্বর্ণকাৰৰ ভাও ধৰি ঘৰে ঘৰে ঘূৰি ফুৰিছিল। তেওঁ ম্লান পৰি যোৱা অলঙ্কাৰৰ চিকমিকনি পুনৰ ঘূৰাই অনাৰ প্ৰতিশ্ৰুতি দি ফুৰিছিল। এগৰাকী মহিলাই কোনো সন্দেহ নকৰি হাতৰ খাৰুযোৰ খুলি তেওঁক দিছিল। মানুহজনে খাৰুযোৰ এটা বিশেষ দ্ৰাৱকত ডুবাই ধৰিছিল। খাৰুযোৰ নতুনৰ লেখিয়াকৈ উজ্জ্বল হৈ পৰিছিল; পিছে খাৰুযোৰৰ ওজন বহুখিনি কমি গৈছিল। মহিলাগৰাকী অপ্ৰস্তুত হৈ পৰিছিল আৰু অনর্থক বাকবিতণ্ডাৰ মূৰকত মানুহজন সেই ঠাইৰ পৰা পলাইছিল। মানুহজনে ব্যৱহাৰ কৰা দ্ৰাৱকটো কি আছিলে অনুমান কৰি কব পাৰিবা নে ?
উত্তৰ : পৰীক্ষাৰ বাবে important নহয়।
16. গৰম পানীৰ জলাধাৰ (hot water tanks) তৈয়াৰ কৰিবলৈ কপাৰ ব্যৱহাৰ কৰা হয়। কিন্তু ষ্টিল (আইনৰ সংকৰ ধাতু) ব্যৱহাৰ কৰা নহয়। কিয়?
উত্তৰ : কাৰণ— কপাৰে ঠাণ্ডা পানী, গৰম পানী নাইবা জলীয় বাষ্প পানীৰ কোনো এটা অৱস্থাৰ লগতেই বিক্ৰিয়া নকৰে।
Updated on 13th November 2024By :- J.A.C (B.Sc Honours | Web/App Developer.)


.jpg)







.jpg)























0 Comments